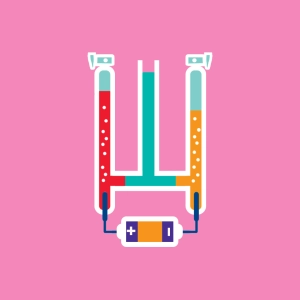
 Electrolyse de l'eau
Electrolyse de l'eau
L'électrolyse (du grec lysis = délier, dissoudre) est la décomposition d'un élément chimique sous l'effet d'un courant électrique.
Le voltamètre d'Hoffmann est le dispositif expérimental permettant d'étudier l'électrolyse de l'eau. On parle d'électrolyse de l'eau, mais, pour assurer une bonne conductivité électrique, l'eau pure ne suffit pas et on doit ajouter un électrolyte, comme de l'acide sulfurique H2SO4.
Sous l'action d'une différence de potentiel de quelques volts, une réaction électrochimique apparaît au niveau des électrodes :
La cathode délivre des électrons qui décomposent l'eau selon la réaction de réduction :
2H2O + 2e- → H2 + 2OH-
Côté anode, les molécules d'eau subissent la réaction d'oxydation suivante :
2H2O → O2 + 4H++ 4e-
Le bilan donne l'équation de décomposition suivante :
2H2O → O2 + 2H2
La réaction produit deux fois plus de dihydrogène que de dioxygène. La loi d'Avogadro justifie que le volume de gaz dans le tube de gauche (H2) est deux fois plus important que le volume de gaz récupéré dans le tube de droite (O2).
