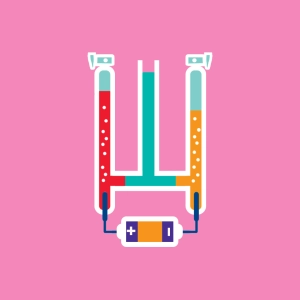
 Elektrolyse van water
Elektrolyse van water
Elektrolyse (van het Griekse lysis = losmaken, vrijmaken) is de ontbinding van een chemische stof door middel van een elektrische stroom.
De voltmeter van Hoffmann is een apparaat om elektrolyse van water te meten. Men spreekt van elektrolyse van water, maar voor een goede elektrische geleiding is zuiver water ongeschikt en moet men een elektrolyt toevoegen, zoals bijvoorbeeld zwavelzuur, H2SO4.
Door de werking van het potentiaalverschil van enkele volts vindt in de buurt van de elektroden een chemische reactie plaats.
Bij de kathode komen elektronen vrij die water ontbinden volgens de reductiereactie:
2H2O + 2e- → H2 + 2OH-
Aan de kant van de anode ondergaan de watermoleculen de volgende oxydatiereactie:
2H2O → O2 + 4H++ 4e-
Gecombineerd levert dit de reactievergelijking:
2H2O → O2 + 2H2
De reactie levert tweemaal zoveel waterstof als zuurstof op. Op grond van de wet van Avogadro is het volume van het gas in de linkerbuis (H2) tweemaal zo groot als het volume van het herwonnen gas in de rechterbuis (O2).
