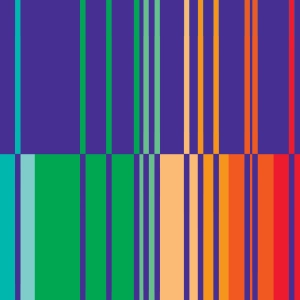
 Emissie- en absorptiespectra
Emissie- en absorptiespectra
Een prisma (of een rij prisma’s) worden gebruikt om een lichtbundel te splitsen in zijn verschillende frequenties.
Het verkregen spectrum kan continu of discreet zijn (‘lijnspectrum’).
Een van de belangrijkste ontdekkingen van de quantummechanica is dat de energie van een atoom uitsluitend bepaalde vaste waarden kan hebben. Ze is ‘gekwantiseerd’ (zie de animatie over het lijnspectrum van het waterstofatoom). Hierdoor kan een gas bestaande uit één atoom een beperkt aantal frequenties uitzenden of absorberen.
Bij een gegeven element heeft het emissiespectrum (bovenste gedeelte van de animatie) dezelfde frequentie als het absorptiespectrum (onderste gedeelte).
Bron voor de waarden van de spectraallijnen: CDS Strasbourg University (link) uit Reader J., en Corliss Ch.H. CRC Handbook of Chemistry and Physics; NSRDS-NBS 68 (1980).
