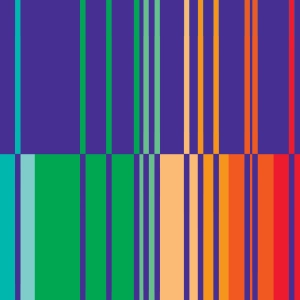
 Spectre d'émission et d'absorption
Spectre d'émission et d'absorption
Un prisme (ou un réseau) permet de décomposer un rayon de lumière en fonction de ses différentes fréquences.
Le spectre lumineux obtenu peut être continu ou discret (spectre de raies).
Une des grandes découvertes de la mécanique quantique est que l'énergie d'un atome ne peut prendre que certaines valeurs bien déterminées. Elle est « quantifiée » (voir l'animation spectre de raie de l'atome d'hydrogène). Pour cette raison, un gaz composé d'un seul atome ne peut absorber ou émettre qu'un nombre limité de fréquences.
Pour un même élément, le spectre d'émission (partie supérieure de l'animation) possède les mêmes fréquences que son spectre d'absorption (partie inférieure).
Source pour les valeurs des raies spectrales : CDS Université de Strasbourg (lien) d'après Reader J., and Corliss Ch.H. CRC Handbook of Chemistry and Physics; NSRDS-NBS 68 (1980). programmation Adrien Willm.
